Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
福崎 裕延*; 吉田 勝; 浅野 雅春; 熊倉 稔; 真下 透*; 湯浅 久子*; 今井 強一*; 山中 英寿*
Makromol. Chem., 191, p.731 - 736, 1990/04
Mn=1600-4800の非晶性コポリマーをL-乳酸(LA)とDL-ヒドロキシイソカプロン酸(HICA)の無触媒・直接脱水縮合反応によって合成した。このコポリマーはdrog delivery systemへの応用に対し生分解型材料として有用である。この場合、in vivo分解パターンはポリマーの分子量と密接に関係しており、分子量の増加によってそのパターンが放物線型からS-字型へと変化することが分かった。LH-RH類似物質(des-Gly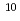 -[D-Len
-[D-Len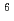 ]-LH-RH ethylamide)を圧融着法によって針状に成形したポリマー中に複合化し、その複合体針のin vivo性能を動物実験から評価した。S-字型分解・放出パターンからなるCopoly(LA/HICA,70/30mol-%)(Mn=2200)複合体針の場合、血清薬物濃度は15週の実験期間を通して、約3.5ng/mlで一定レベルを維持した。
]-LH-RH ethylamide)を圧融着法によって針状に成形したポリマー中に複合化し、その複合体針のin vivo性能を動物実験から評価した。S-字型分解・放出パターンからなるCopoly(LA/HICA,70/30mol-%)(Mn=2200)複合体針の場合、血清薬物濃度は15週の実験期間を通して、約3.5ng/mlで一定レベルを維持した。
浅野 雅春; 福崎 裕延*; 吉田 勝; 熊倉 稔; 真下 透*; 湯浅 久子*; 今井 強一*; 山中 英寿*
Drug Des. Delivery, 5, p.301 - 320, 1990/00
1400-16900の数平均分子量(Mn)をもつDL-乳酸ポリマー(PLA)を合成し、それのin vivo分解パターンを動物の背中皮下に埋め込むことによって調べた。Mnが1600以下のPLAでは、その分解パターンは放物線型で、Mn=2000以上になると分解に誘導期を示すS-字型になることが分かった。この場合、S-字型分解パターンに見られる誘導期はMnに強く依存し、Mnが大きくなると、より長期間になる傾向を示した。これらのポリマー担体に薬物を包括し、担体のin vivo分解パターンと薬物のin vivo放出パターンの関係および動物の前立腺におよぼす薬理作用についても調べた。放物線型のin vivo分解パターンをもつPLAの場合、薬物のin vivo放出は数週間以内で殆ど完結した。これに対し、S-字型のそれは、初期段階にみられる薬物の急激な放出を抑制できることが判明した。結果的に、最も強い薬理効果はMn=2000のPLA系で12週の期間にわたって観察された。
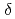 -valerolactone with relatively low molecular weight for application in drug delivery systems
-valerolactone with relatively low molecular weight for application in drug delivery systems福崎 裕延*; 吉田 勝; 浅野 雅春; 熊倉 稔; 真下 透*; 湯浅 久子*; 今井 強一*; 山中 英寿*; 河原田 うめ子*; 鈴木 慶二*
Journal of Controlled Release, 10, p.293 - 303, 1989/00
Mn=1500-2600のCopoly(L-lactic acid/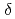 -valerolactone)(copoly(LA/VL))をDDSのための生分解性担体として用いるため、無触媒下で直接脱水縮合によって合成した。LA組成を関数として、固体状(100-80mol-%LA)、ペースト状(70-30mol%LA)、そしてワックス状(15-0mol-%LA)ポリマーを得た。Rhizopus delemer lipaseは最も高い分解活性を示した。この場合、ペースト状ポリマーの分解速度は、固体、ワックス状ポリマーのそれより著るしく速い。estradiol-17
-valerolactone)(copoly(LA/VL))をDDSのための生分解性担体として用いるため、無触媒下で直接脱水縮合によって合成した。LA組成を関数として、固体状(100-80mol-%LA)、ペースト状(70-30mol%LA)、そしてワックス状(15-0mol-%LA)ポリマーを得た。Rhizopus delemer lipaseは最も高い分解活性を示した。この場合、ペースト状ポリマーの分解速度は、固体、ワックス状ポリマーのそれより著るしく速い。estradiol-17 のnitrogen mustard誘導体であるestramustineをMn=2500をもつcopoly(LA/VL、70/30mol-%)(ペーストポリマー)の中に均一分散固定した。この系は、in vivo実験系において、埋入から5週目で完全分解消失する。rat prostateにおよぼす薬理作用は、5週の期間にわたって観察された。
のnitrogen mustard誘導体であるestramustineをMn=2500をもつcopoly(LA/VL、70/30mol-%)(ペーストポリマー)の中に均一分散固定した。この系は、in vivo実験系において、埋入から5週目で完全分解消失する。rat prostateにおよぼす薬理作用は、5週の期間にわたって観察された。
吉田 勝; 浅野 雅春; 嘉悦 勲; 今井 強一*; 湯浅 久子*; 山中 英寿*; 志田 圭三*; 鈴木 慶二*; 若林 克己*; 山崎 巖*
Polym.J., 18(4), p.287 - 296, 1986/00
被引用回数:9 パーセンタイル:51.88(Polymer Science)低温放射線注形重合法によって、疎水性diethylene glycol dimethacrylate/親水性polyethylene glycol #600 dimethacrylateからなる80/20 vol-%組成のメタクリル酸コポリマー中にdes-Gly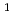
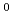 -[D-Leu
-[D-Leu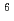 ]-LH-RH-ethlamideを包含する。上述の薬物は水に可溶である。一般にポリマー中に単純分散状態で包含されている薬物のin vitro放出パターンは時間を関数とした時、イクスポネンシャルな減少傾向を示す。本稿では、コポリマーからの薬物の放出に見掛け上zero-order mechanismを付与するため、薬物を錠剤化(加圧下)し、それの上下に適当なフィルター膜を重ね合わせ、さらにメタクリル酸コポリマーによって含浸包含することを試みた。例えば、Whatman No.1フィルター膜を用いた場合、複合体からの薬物のin vitro放出パターンは見掛け上zero-order mechanismをとり、250日間の試験期間にわたって16
]-LH-RH-ethlamideを包含する。上述の薬物は水に可溶である。一般にポリマー中に単純分散状態で包含されている薬物のin vitro放出パターンは時間を関数とした時、イクスポネンシャルな減少傾向を示す。本稿では、コポリマーからの薬物の放出に見掛け上zero-order mechanismを付与するため、薬物を錠剤化(加圧下)し、それの上下に適当なフィルター膜を重ね合わせ、さらにメタクリル酸コポリマーによって含浸包含することを試みた。例えば、Whatman No.1フィルター膜を用いた場合、複合体からの薬物のin vitro放出パターンは見掛け上zero-order mechanismをとり、250日間の試験期間にわたって16 g/dayの一定値を保持した。これはradioimmuno assayから測定したserum薬物濃度の値からも示唆される。
g/dayの一定値を保持した。これはradioimmuno assayから測定したserum薬物濃度の値からも示唆される。
吉田 勝; 浅野 雅春; 嘉悦 勲; 山田 英寿*; 中井 克幸*; 湯浅 久子*; 志田 圭三*
J.Biomed.Mater.Res., 19, p.615 - 629, 1985/00
被引用回数:7 パーセンタイル:40.17(Engineering, Biomedical)放射線重合法によって作った徐放性機能をもつホルモン含有針状(0.8mm径,3mm長)ビニルポリマー複合体をラットの背中皮下,睾丸,そして右葉の前立腺腹葉に挿入した。埋入箇所と薬理作用(SV,DLP,VP,Ad、Tの重量変化を尺度)の関係を、最高12W埋入することによって検討した。AA560を用いた時の薬理作用は皮下埋入が著明で、次いで睾丸そして前立腺腹葉の順であった(36 g daily,in vitro放出量)。同じ傾向はEstracyt(R)を用いた時にも観察された(15
g daily,in vitro放出量)。同じ傾向はEstracyt(R)を用いた時にも観察された(15 g)。埋入箇所に依存した薬理作用の違いはE
g)。埋入箇所に依存した薬理作用の違いはE -17
-17 を用いた時に出現しなかった。しかし、この複合体は用いた薬物の中で最も強い作用を示した(6
を用いた時に出現しなかった。しかし、この複合体は用いた薬物の中で最も強い作用を示した(6 g)。一方、CMA含有複合体系の場合(28
g)。一方、CMA含有複合体系の場合(28 g)薬理作用は埋入箇所が異っているにもかかわらず全く出現しなかった。上述した結果と薬物を単に経口・静注した時の結果についても検討を加えた。
g)薬理作用は埋入箇所が異っているにもかかわらず全く出現しなかった。上述した結果と薬物を単に経口・静注した時の結果についても検討を加えた。
嘉悦 勲; 吉田 勝; 浅野 雅春; 志田 圭三*; 山中 英寿*; 中井 克幸*; 湯浅 久子*; 鈴木 慶二*; 若林 克己*; 白石 明*; et al.
人工臓器, 13(3), p.1168 - 1171, 1984/00
前立腺等の泌尿器官に薬理(萎縮)作用を有し、ホルモン療法剤として注目されているLH-RH類似物質(アナログ)を放射線重合により親水性アクリレートと疎水性アクリレートの共重合体中に固定化し、その長期リリース挙動、薬理作用などを検討した。担体からのLH-RHアナログの溶出は100日~200日にわたってコンスタントに続き、微量のけ中濃度レベルを維持することがインビトロ実験ならびにラット実験から明らかになった。また前立腺等に対する萎縮効果もラット実感から確かめられた。副作用や異物反応はほとんど認められなかった。この方法は注射投与を頻繁に継続するよりもはるかに筒便で有効であり、臨床的適用性が高いものと判断され、今後前立腺癌の治療法としての発展が期待される。
 2,100)の作用
2,100)の作用吉田 勝; 浅野 雅春; 嘉悦 勲; 山中 英寿*; 中井 克幸*; 志田 圭三*
高分子論文集, 41(3), p.145 - 150, 1984/00
被引用回数:1 パーセンタイル:14.35(Polymer Science)ポリエチレングリコール(Mn=1900-2100)を含む徐放性テストステロン複合体を去勢したウイスター系ラットの背中皮下に最高で90日間にわたって埋入した。埋入から7,30,90日目に複合体から放出されたテストステロンのin vivo累積量は各々498,2120,6913 gであった。これはポリエチレングリコールを含まない複合体系のin vivo累積放出量より約3.2倍増加した。一方、ポリエチレングリコールを含む複合体系のin vivoとin vivoにおける累積放出量を比較した場合、in vivoより約2倍高い値を示した。このことから、ポリエチレングリコールが生体組織内における薬物の透過・拡散(輸送)を促進する物質として働いていると結論した。これは血清テストステロン濃度および前立腺腹葉の重量変化を尺度とした薬理作用の結果からも示唆される。
gであった。これはポリエチレングリコールを含まない複合体系のin vivo累積放出量より約3.2倍増加した。一方、ポリエチレングリコールを含む複合体系のin vivoとin vivoにおける累積放出量を比較した場合、in vivoより約2倍高い値を示した。このことから、ポリエチレングリコールが生体組織内における薬物の透過・拡散(輸送)を促進する物質として働いていると結論した。これは血清テストステロン濃度および前立腺腹葉の重量変化を尺度とした薬理作用の結果からも示唆される。
嘉悦 勲; 吉田 勝; 浅野 雅春; 山田 明夫*; 桜井 靖久*; 中村 光司*; 高崎 健*; 羽生 富士夫*; 中井 克幸*; 山中 英寿*; et al.
人工臓器, 12(2), p.689 - 692, 1983/00
MMC-高分子複合体を低温放射線重合法により、またTS-ポリペプチドあるいはTS-タンパク質複合体を加圧加熱溶解法により試作した。ビニルポリマー系複合体は複合対中の薬物濃度が高いにも拘らず血液障害を認めずかつ抗腫瘍効果を示した。しかしながら、埋入物周辺の癌細胞に対する有効な作用領域は比較的限局性であることが判明した。そこで上述した作用領域を拡大するため、薬物の生体での拡散透過を促進するような物質、例えばUK,PEG,DMSOあるいはSDSを複合体に共存させてその効果を検討した。一方、消化性担体については、放射線照射によって担体の消化速度を早くしたり、あるいは遅くしたりすることが可能であることを見出した。このような担体特性を薬物の情報化に応用し、担体-薬物複合体の試作条件および薬理機能との関連において検討した。
 -グロブリンを含む複合体からのテストステロンのin vivo溶出
-グロブリンを含む複合体からのテストステロンのin vivo溶出浅野 雅春; 吉田 勝; 嘉悦 勲; 中井 克幸*; 山中 英寿*; 志田 圭三*
高分子論文集, 40(9), p.525 - 530, 1983/00
被引用回数:5 パーセンタイル:38.39(Polymer Science)100kg/cm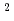 の圧力下で加熱溶触処理の後、
の圧力下で加熱溶触処理の後、 線照射した
線照射した -グロブリン担体をWistan系ラットの背中皮下に埋入した。この担体のin vivo分解は埋入開始から90日目で約1.9%であった。一方、0,0.005,0.01そして0.1W/V%のペプシン溶液を用いた時の担体の37
-グロブリン担体をWistan系ラットの背中皮下に埋入した。この担体のin vivo分解は埋入開始から90日目で約1.9%であった。一方、0,0.005,0.01そして0.1W/V%のペプシン溶液を用いた時の担体の37 Cでのin vitro分解は媒液に浸漬してから90日目で各々1.2,31.4,45.7そして53.9%に達した。これらの結果に基づいて、テストステロンを加圧加熱溶触処理の後、
Cでのin vitro分解は媒液に浸漬してから90日目で各々1.2,31.4,45.7そして53.9%に達した。これらの結果に基づいて、テストステロンを加圧加熱溶触処理の後、 線照射した
線照射した -グロブリン中に複合化した。この場合、担体自体のin vivo分解は薬物の共存によって著しく加速され、90日目で57.4%にまで達した。薬物のin vivo溶出持続期間は本研究の場合、60日が限度であった。さらに、テストステロンのin vivo溶出と薬理作用の関係についても検討した。
-グロブリン中に複合化した。この場合、担体自体のin vivo分解は薬物の共存によって著しく加速され、90日目で57.4%にまで達した。薬物のin vivo溶出持続期間は本研究の場合、60日が限度であった。さらに、テストステロンのin vivo溶出と薬理作用の関係についても検討した。
 -benzyl L-aspartate and
-benzyl L-aspartate and  -methyl L-glutamate for the controlled release of testosterone
-methyl L-glutamate for the controlled release of testosterone浅野 雅春; 吉田 勝; 嘉悦 勲; 山中 英寿*; 志田 圭三*
Makromol.Chem., 184(9), p.1761 - 1770, 1983/00
B-bzL-Asp/ -MeL-Gluのランダムコポリマーを合成し、ラットの皮下に埋入した。このコポリマーはin vivo消化性を有し、かつ生体適合性に優れていることが分った。この結果に基づいて、コポリ(B-bzL-Asp/
-MeL-Gluのランダムコポリマーを合成し、ラットの皮下に埋入した。このコポリマーはin vivo消化性を有し、かつ生体適合性に優れていることが分った。この結果に基づいて、コポリ(B-bzL-Asp/ -MeL-Glu)をdrug delivery systemに対する担体として用いることを試みた。テストステロン/ポリマー複合体は微量のdichloroethane存在下、200kg/cm
-MeL-Glu)をdrug delivery systemに対する担体として用いることを試みた。テストステロン/ポリマー複合体は微量のdichloroethane存在下、200kg/cm の圧力下で試作した。複合体からのテストステロンのin vivo溶出速度はin vitroより約5.5倍大きかった。この場合、in vivo溶出速度は90日間にわたって一定値(0.22mg/day)を示した。去勢ラットに達するserum薬物濃度は0.40ng/mlであったが、複合体埋入系のそれは6.8ng/mlであった。
の圧力下で試作した。複合体からのテストステロンのin vivo溶出速度はin vitroより約5.5倍大きかった。この場合、in vivo溶出速度は90日間にわたって一定値(0.22mg/day)を示した。去勢ラットに達するserum薬物濃度は0.40ng/mlであったが、複合体埋入系のそれは6.8ng/mlであった。